روش اسمز معکوس در تصفیه آب
روش اسمز معکوس در تصفیه آب
روش اسمز معکوس در تصفیه آب(Reverse Osmosis) یکی از شیوههای گسترده جداسازی است، که کاربریهای مختلفی دارد. شیرین سازی آب دریا، جداسازی مواد آلی و سمی از پسابهای صنعتی دو مورد مهم استفاده از این تکنولوژی میباشد. اسمز معکوس یکی از روشهای اصلی شیرین سازی آب در کنار روشهایی مانند تقطیر، الکترودیالیز، بدون یونسازی و… است که در مقیاسهای آزمایشگاهی؛ شهری و صنعتی مورد استفاده قرار میگیرد.
تاریخچه کاربرد روش اسمزی معکوس به سالهای 1950 بر میگردد که آزمایشهایی توسط رید و برتون در دانشگاه فلوریدای آمریکا انجام پذیرفت و نخستین غشاء اسمزی معکوس از سلولز استات ساخته شد و در اواخر سالهای 1960 این پدیده به صورت تجاری مورد استفاده قرار گرفت.
اصول نظری پدیده اسمز معکوس
شناخته پدیده اسمز معکوس نیازمند شناسایی خاصیت اسمزی است. به طور کلی انتقال جرم از یک محیط به محیط دیگر در اثر اختلاف غلظت و یا به عبارت بهتر در اثر اختلاف پتانسیل شیمیایی، به وجود میآید. به عنوان مثال ظرف آبی را در نظر بگیرید که یک قطعه بلور نمک طعام به درون آن انداخته میشود. در بخشی از ظرف که بلور نمک وجود دارد، غلظت نمک زیاد وغلظت آب ناچیز است و در بخش دیگر ظرف غلظت نمک صفر و غلظت آب بسیار زیاد است. در اثر اختلاف غلظت، ملکولهای بلور نمک، نفوذ به بخش دیگر را که آب است، آغاز مینمایند و از سوی دیگر مولکولهای آب نیز به بخش بلور نمک نفوذ میکند. این عمل تا یکسان شدن غلظت آب و نمک در دو بخش ادامه مییابد. چون بعد از آن نیروی محرکه که همان اختلاف غلظتی است بین دو محیط وجود ندارد و به بیان دیگر حالت تعادل برقرار گردیده است.
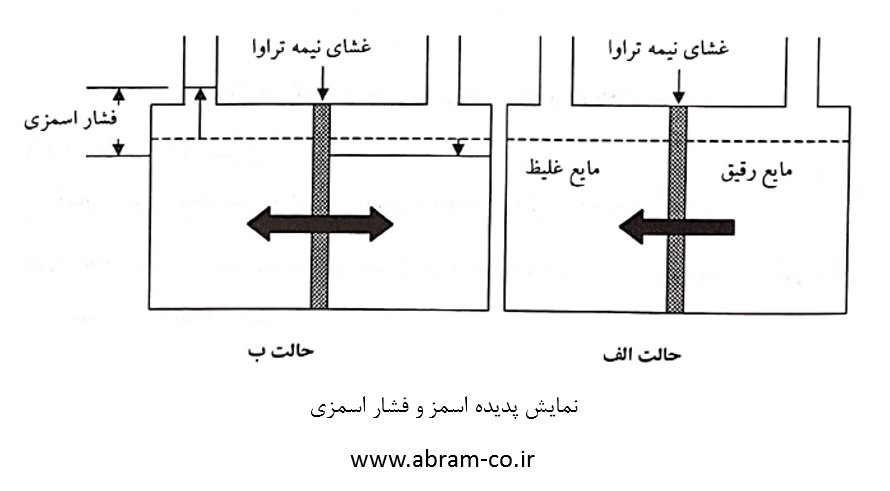
خاصیت اسمزی به عبور یک حلال از بخش محلول رقیق به بخش محلول غلظت از درون یک غشاء نیمه تراوا گفته میشود. برای تشریح این ویژگی، شکل بالا که نشان دهنده ظرفی شامل دو بخش و یک غشاء میباشد، را در نظر بگیرید. آب و یا محلول رقیق آب نمک در یک بخش، محلول غلیظ آب نمک در بخش دیگر و غشایی که تنها به ملکول آب اجازه عبور میدهد. غشاء از عبور یونهای تشکیل دهنده نمک به دلیل بزرگ بودن جلوگیری مینماید.
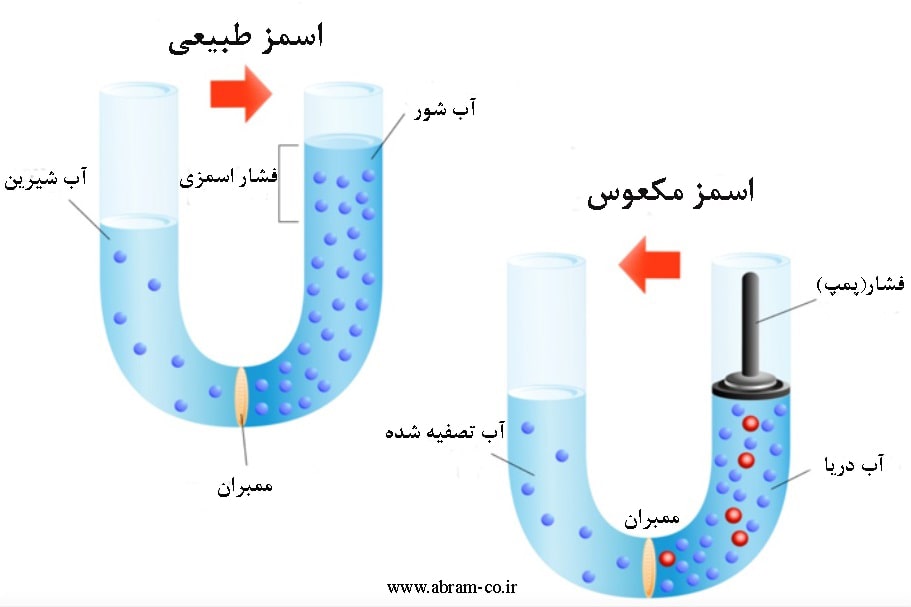
درابتدا سطح مایعات در دو بخش مساوی میباشند به دلیل وجود تمایل به یکسان نمودن غلظتها در دو بخش، مولکولهای آب از بخش محلول رقیق از غشاء عبور نموده و به درون محلول غلیظ نفوذ میکند. سطح مایع در بخش غلیظ افزایش مییابد. جریان مولکولهای آب از درون غشاء تا آنجا انجام میگیرد که اختلاف سطح مایع ( به عبارتی دیگر اختلاف فشار) در دو بخش مانع حرکت مولکولهای آب شود. اختلاف فشار در بخش جداشده توسط غشاء که در آن از جریان خالص مولکولهای آب جلوگیری مینماید، را فشار اسمزی مینامند. فشار اسمزی سبب ایجاد تعادل در دو بخش میشود. حال چنانچه فشاری بیش از فشار اسمزی به بخش محلول غلیظ وارد شود، عکس پدیده اسمزی بروز میکند، به عبارت دیگر مولکولهای آب از بخش محلول غلیظتر به بخش محلول رقیقتر جریان مییابد. این پدیده را اسمز معکوس مینامند.
از پدیده اسمز معکوس برای تصفیه آب و به عبارت کلیتر برای فرایند تغلیظ و جداسازی استفاده میشود. فشار اسمزی با غلظت املاح موجود در محلول نسبت مستقیم دارد. به عنوان مثال در محلول ابکی نمک طعام افزایش غلظت به مقدار هر میلیگرم در لیتر سبب زیاد شدن فشار اسمزی به میزان psi01/0 میشود. دقت شود که در اثر عبور مولکولهای آب از غشاء، غلظت یونهای محلول پشت غشاء به تدریج افزایش یافته و در نتیجه فشار اسمزی نیز زیاد میشود.

محاسبه فشار اسمزی روش اسمز معکوس در تصفیه آب
فشار اسمزی ایجاد شده از املاح محلول توسط دو روش محاسبه میگردد.
- رابطه وانتف: وانتف تابعیت فشار اسمزی را متناسب با غلظت املاح محلول و دمای مطلق محلول بیان نموده است.

ضریب فشار اسمزی در رابطه وانتف تابع غلظت املاح و دما است. برای محلول 0.1 مولار برخی از نمکها در دمای C° 20 به صورت جدول زیر است.
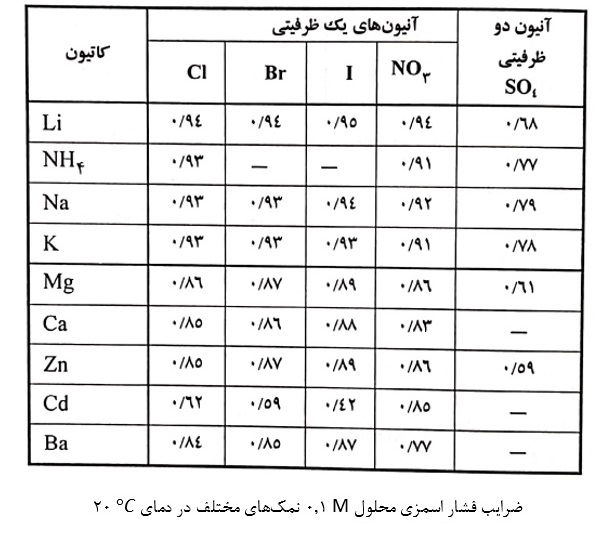
- روش فاکتور اسمزی (osmosic pressure factor)
فرمول زیر شیوه سادهتری برای محاسبه فشار اسمزی توسط روش فاکتور اسمزی در اختیار میگذارد.

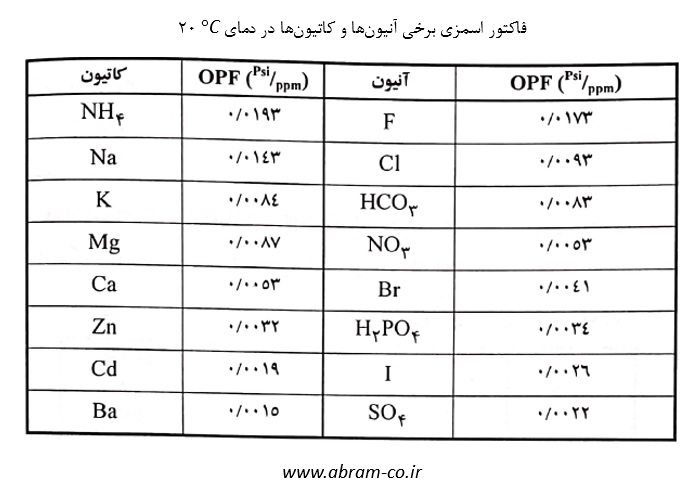
با توجه به مقادیر فاکتور اسمزی برای یونهای مختلف در جدول زیر ، فشار اسمزی محلول محاسبه میشود.
محاسبه شدت جریان حلال عبوری از غشا
شدت جریان حلال عبوری از غشاء تابع تفاوت اختلاف فشار اعمال شده و فشار اسمزی محلول، سطح غشاء و ضریب نفوذ پذیری حلال در غشاء است.

محاسبه جریان عبوری ماده حل شده از غشاء
شدت جریان عبوری ماده حل شده از غشاء تابع اختلاف غلظت جزء حل شونده محلول ورودی به غشاء و محلول خروجی از غشاء، سطح غشاء و ضریب نفوذپذیری ماده حل شونده از غشاء است.